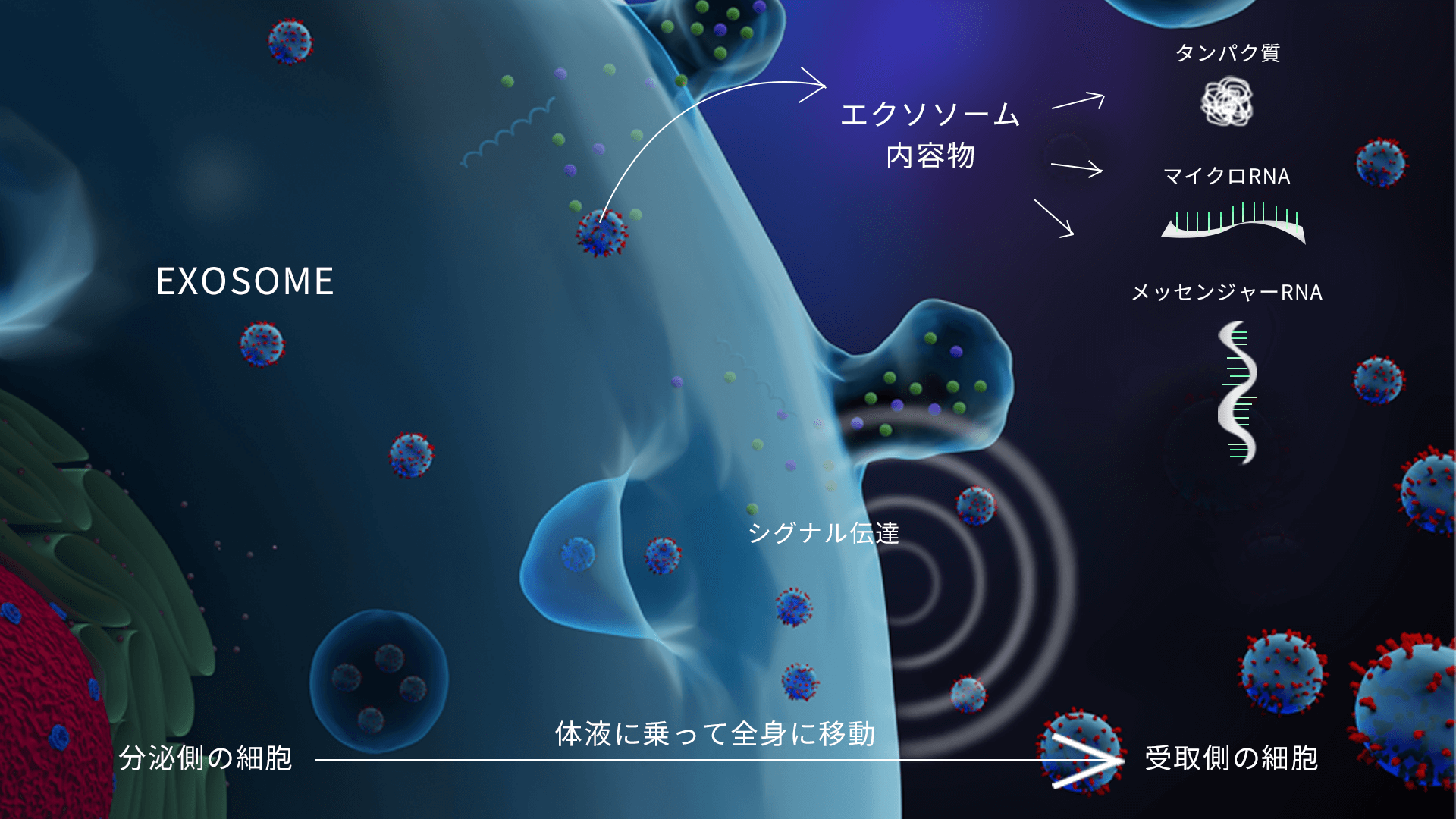
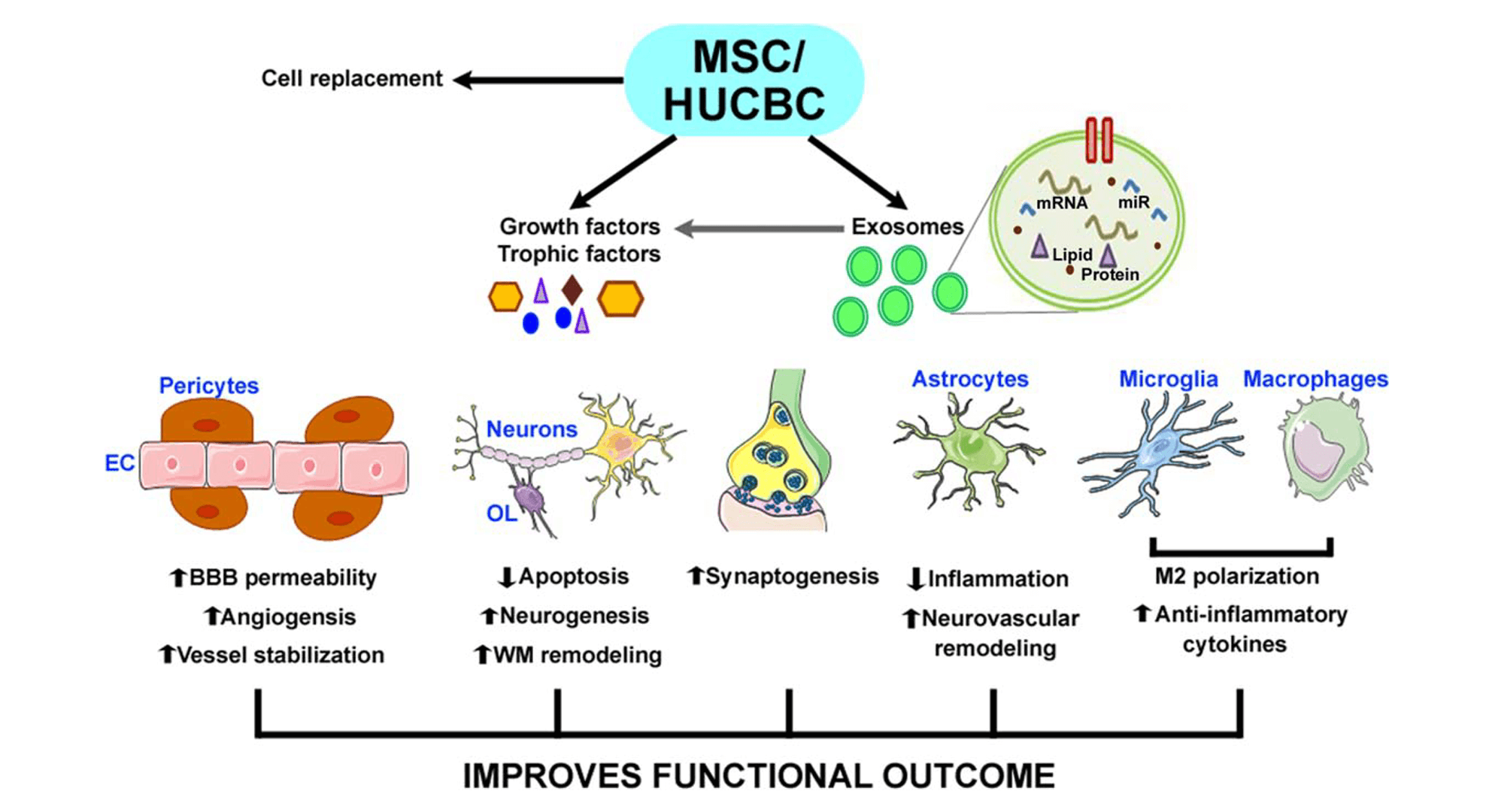
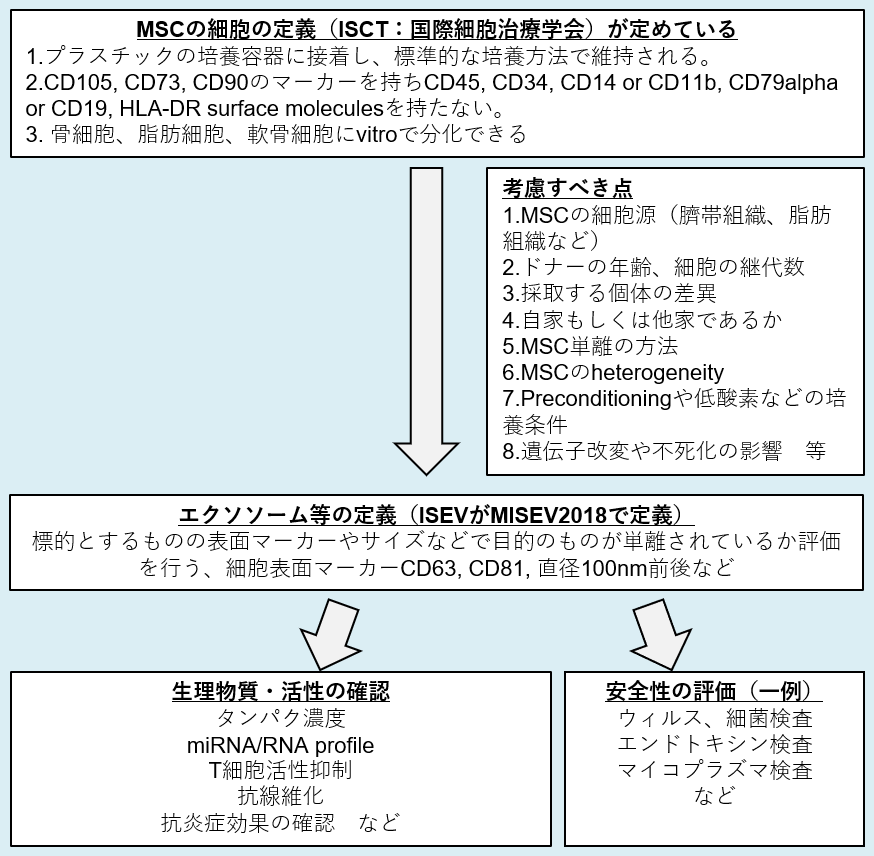
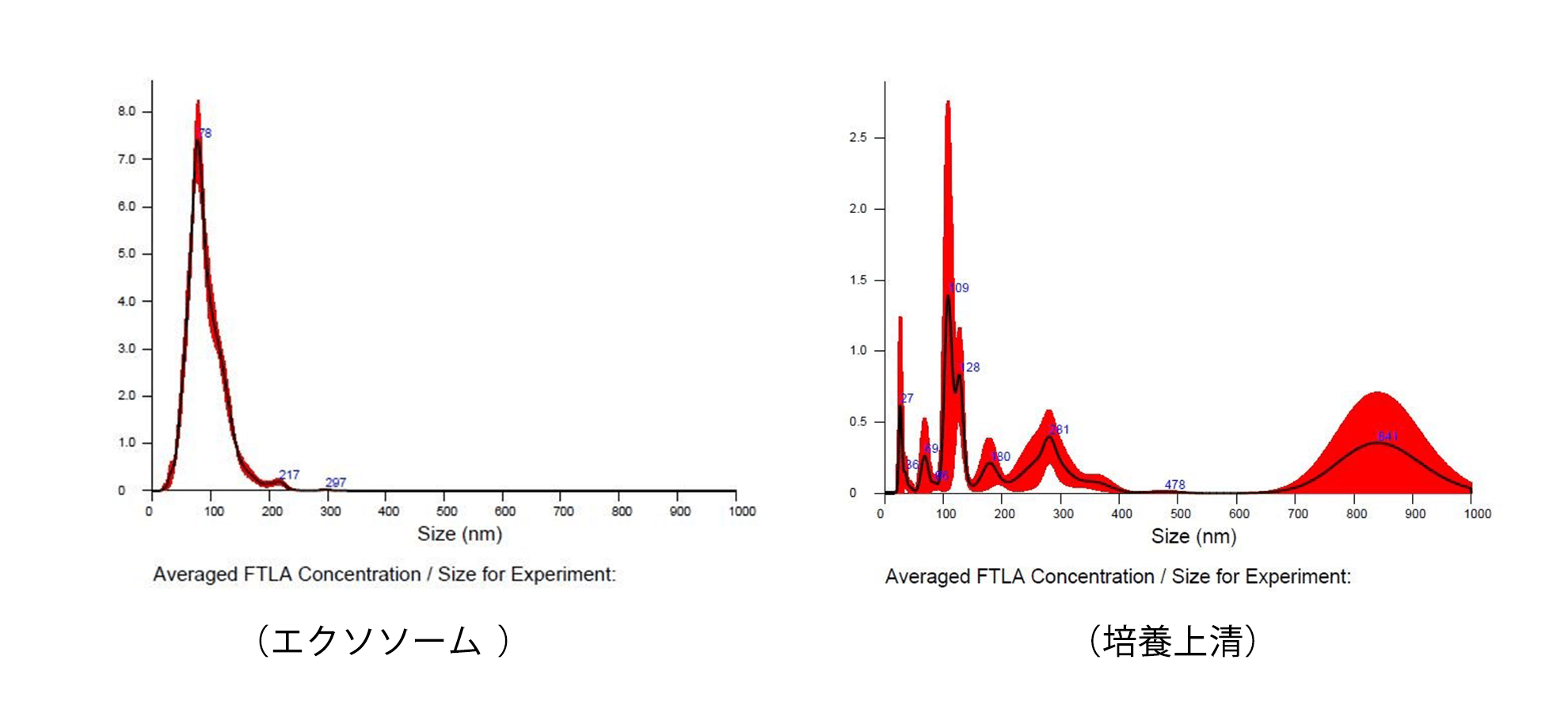
エクソソームの仕組み
エクソソームの内部にはマイクロRNAという短い遺伝子配列が入っている。マイクロRNAには端的な情報が書かれており、その情報こそが幹細胞の効果ではないかと言われている。UC Sandiego 大学の研究では「幹細胞は脱核させても同じような薬理効果がある」ことを報告しており、それは幹細胞の薬理作用の本体はエクソソーム等のEVであるということを意味する。。また、エクソソームは細胞に由来する自然由来であり、すでに人体内に多く存在していて副作用が低いとされ、細胞治療と比べても優位性も認識されるようになっている。