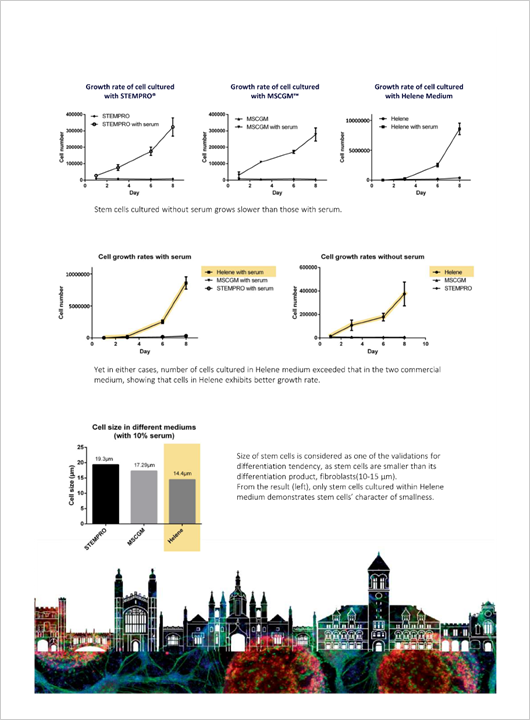
Năm 2018, tại Hội nghị chuyên đề về Tế bào gốc Quốc tế Cambridge, chúng tôi đã trình bày thành tựu nghiên cứu về môi trường nuôi cấy tự tạo không chứa huyết thanh và yếu tố động vật (HELENE Medium). Điểm đầu tiên, so với các cơ sở hiện có khác, trong cùng một khoảng thời gian, HELENE Medium có thể nuôi cấy nhiều hơn về số lượng tế bào. Điểm thứ hai, có thể quan sát thấy kích thước tế bào nhỏ nhất trong số ba môi trường. Trong đó, kích thước Tế bào gốc trung mô được nuôi cấy trong HELENE Medium là nhỏ nhất. Bằng chứng khoa học cho thấy các tế bào gốc càng nhỏ, càng ít có khả năng biệt hóa thành nguyên bào sợi.
Dựa hai điểm trên, có thể nhận định rằng mô mỡ được lấy từ phía sau tai có chứa MSC (tế bào gốc trung mô). Tuy lượng mô mỡ thu được khi lấy mẫu ít hơn so với phần đùi và phần bụng, nhưng với công nghệ phòng thí nghiệm độc quyền của chúng tôi và HELENE Medium, trong một tháng, có thể nuôi cấy tới 2,25 tỷ MSC.

Để đảm bảo chất lượng tế bào gốc cung cấp cho khách hàng, chúng tôi đã ủy thác cho bên thứ ba tiến hành thử nghiệm kiểm tra các mẫu tế bào gốc được sản xuất theo đúng quy trình tương tự như giấy Chứng nhận chất lượng này. Thử nghiệm tuân thủ GMP (Good Manufacturing Practice), GLP (Good Manufacturing Practice) và bao gồm thêm ba thử nghiệm được thiết kế riêng khác. Chúng tôi cung cấp tế bào sau khi tiến hành các xét nghiệm tương đương trong phòng thí nghiệm riêng của chúng tôi, cùng với kết quả xác minh chất lượng tế bào gốc của các công ty thuốc thử bên thứ ba, cung cấp thông tin cho bệnh nhân một cách công bằng, minh bạch như mô tả dưới đây.
Mô mỡ của ba người hiến mẫu sau khi được nuôi cấy tại phòng thí nghiệm của chúng tôi được gửi đi thử nghiệm kiểm tra. Mẫu mô được lấy từ phía sau tai, sau đó được phân tách và chia nhỏ bằng kỹ thuật đặc biệt và các enzyme chuyên dụng. Các tế bào được chia thành đơn bào, sau đó được nuôi cấy trong một tháng, khi đạt đến số lượng quy định sẽ được phân tách bằng MACS. Sau khi xác nhận số lượng tế bào bằng bộ đếm tế bào, chúng được cung cấp cho công ty Takara Bio Inc, một công ty thuốc thử bên thứ ba.

| Mục đích | Tên xét nghiệm | Mẫu XN | Kết quả |
|---|---|---|---|
| Nhiễm khuẩn và nhiễm bệnh |
Kiểm tra vô trùng (Dược điển Nhật Bản Phương pháp Trực tiếp, Tùy chọn: Kiểm tra tính phù hợp của phương pháp) |
QC_AL Lot:#13349 | Âm tính |
| Kiểm tra vô trùng (Dược điển Nhật Bản Phương pháp Trực tiếp) |
QC_AL Lot:#13349 | Âm tính | |
| Kiểm tra loại trừ Mycoplasma (Thông tin tham khảo Dược điển Nhật Bản, Phương pháp PCR (có xác nhận 7 loài bị ức chế)) |
QC_AL Lot:#13349 | Âm tính | |
| Kiểm tra nội độc tố (Dược điển Nhật Bản Phương pháp Đo đục động học, Tùy chọn: Kiểm tra yếu tố gây can thiệp) |
QC_AL Lot:#13349 | Âm tính | |
| Kiểm tra nội độc tố (Dược điển Nhật Bản Phương pháp Đo đục động học) |
QC_AL Lot:#13349 | Ít hơn độ chính xác phát hiện | |
| Hình thành khối u | Kiểm tra hình thành khuẩn lạc | QC_AL Lot:#13349 | Âm tính |
| Xác nhận tế bào gốc | Kiểm tra FCM (CD45- CD105+) |
QC_AL Lot:#13349 | CD45- 92.1% CD105+ 100% |
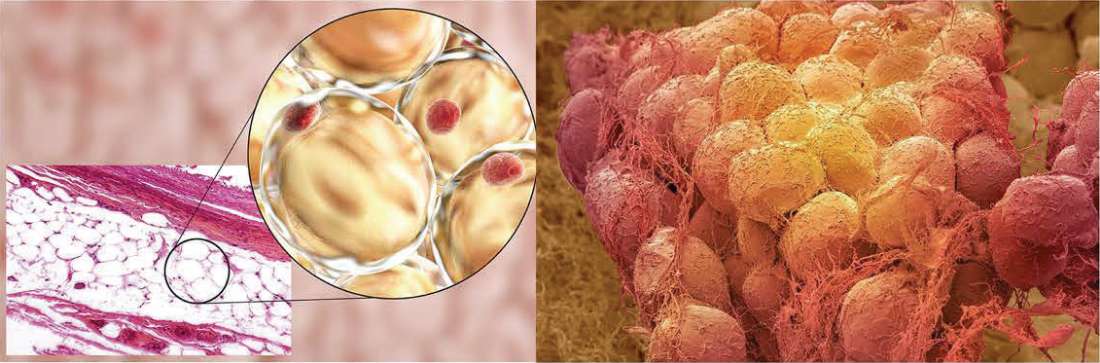
Trên đây là hình ảnh biểu thị tổ chức mô mỡ, vật thể trong giống như hạt đậu đó chính là mô mỡ. Tế bào gốc ẩn trong một khu vực giống như mạng lưới sợi được gọi là hốc tế bào gốc. Nói cách khác, tế bào gốc không có trong các giọt lipid mà có ở các vùng xơ xung quanh.
Chúng ta hãy cùng so sánh sự khác biệt giữa mô mỡ ở sau tai và ở bụng.
| Mô mỡ phía sau tai | Mô mỡ dưới da bụng | |
| Hình ảnh quan sát | 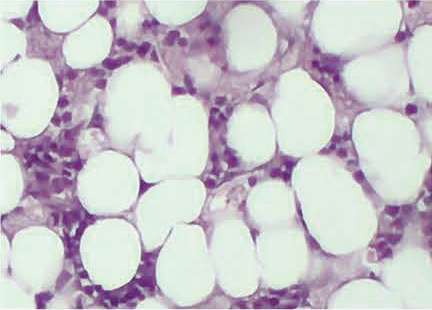 |
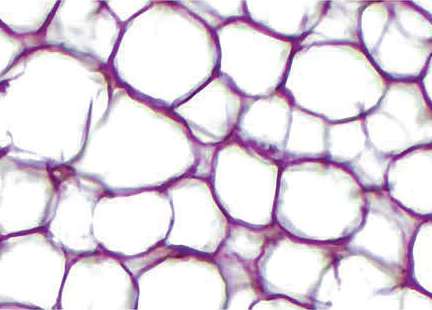 |
| Hình ảnh | 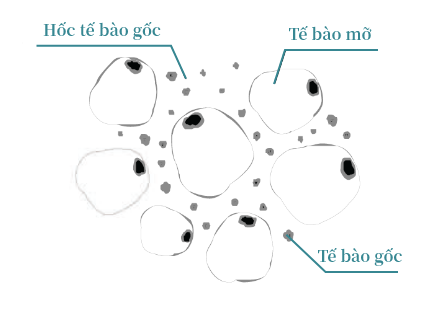 |
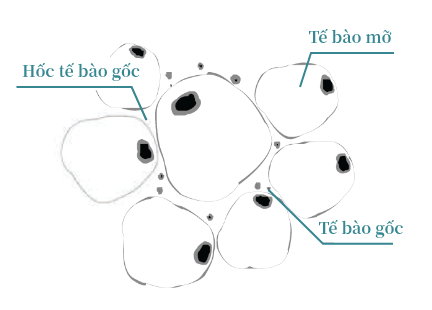 |
| Mức độ đau | Hơi đau | Rất đau (đau bầm tím) |
| Xuất huyết trong | Rất ít | Nhiều |
| Cầm máu | Chỉ cần dùng băng cá nhân | Dùng gạc |
Tế bào gốc có nguồn gốc từ mô mỡ không nằm trong các giọt lipid màu vàng,
Chúng nằm ẩn xung quanh các giọt lipid (= hốc tế bào gốc) được gọi là stroma.
Tế bào gốc tồn tại ở cả mỡ bụng và mỡ sau tai, tuy nhiên tại “vùng mỡ có ít giọt lipid hơn và nhiều kẽ hơn” thì có tỷ lệ tế bào gốc cao hơn.
Tại Helene, chúng tôi chủ yếu lấy mỡ sau tai nên ít gây đau đớn cho bệnh nhân.
Tuy nhiên, đối với những người có nguyện vọng lấy mẫu ở bụng cũng có thể áp dụng phương pháp hút mỡ bụng để tiến hành lấy mẫu.
Tế bào gốc được nuôi cấy tại Trung tâm tế bào HELENE (HELENE Cell Center) được đo ít nhất trong hai giai đoạn để xác nhận số lượng và khả năng sống của tế bào gốc trước khi truyền vào cơ thể khách hàng. Kết quả được phòng thí nghiệm xác nhận và in ra. Chúng tôi phục vụ mọi khách hàng một cách khoa học và có trách nhiệm.

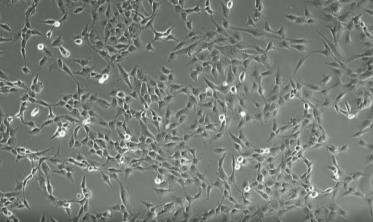
Sau khi lấy được mẫu tế bào, quá trình nhuộm được thực hiện bằng cách thêm dung dịch tyban blue 0,4%, một chất nhuộm quan trọng thường được sử dụng để phân biệt tế bào sống và tế bào chết. Phương pháp nhuộm là thí nghiệm loại trừ sắc tố, dung dịch nhuộm thấm vào các tế bào chết nhưng lại bị chặn bởi màng tế bào của các tế bào sống với mục đích sử dụng để phân biệt, tính toán khả năng sống của tế bào. Thông thường, các mẫu nhuộm được quan sát dưới kính hiển vi và được đếm thủ công, nhưng tế bào tự động sẽ tự động nhận ra phản ứng huỳnh quang và hoàn thành phân tích. Để đếm thủ công, không chỉ phải thực hiện lấy nét thủ công mà còn phải điều chỉnh lượng ánh sáng trường sáng giữa các mẫu. Bộ đếm tế bào tự động Countess II FL có thể tự động điều chỉnh ánh sáng và lấy nét để có chất lượng hình ảnh tối ưu khi sử dụng.
Sau khi định lượng bằng Countess II FL, trung tâm tế bào của chúng tôi đặt các mẫu tế bào lên các phiến kính và thu được hình ảnh tế bào bằng kính hiển vi ZEISS AxioVert.A1. HELENE sử dụng chương trình AI độc quyền đọc hình ảnh để quan sát khung tế bào ở cấp độ tiêu điểm, kết hợp độ dài tiêu cự của kính hiển vi, loại tế bào (MSC) và diện tích mặt cắt ngang của bình nuôi cấy tế bào với mục đích xác định số lượng tế bào, tính tỷ lệ sống của tế bào. Hai bước này, với độ chính xác tính toán gần như 100% và quy trình thực hiện độc đáo không một nơi nào có thể bắt chước được, các tế bào gốc sử dụng trong trị liệu của thương hiệu HELENE được điều chỉnh chính xác theo nhu cầu của khách hàng và không ngừng được tối ưu hóa.
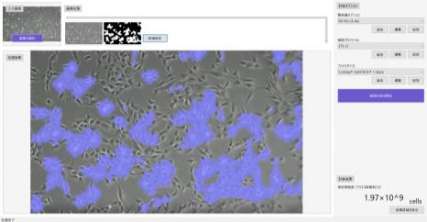
Tại HELENE, chúng tôi thể hiện cam kết về chất lượng và tính minh bạch bằng cách cung cấp Giấy chứng nhận tế bào gốc cho mỗi lần điều trị.
Theo bài báo năm 2021 [Sự an toàn của liệu pháp MSC trong 15 năm qua: Một phân tích tổng hợp], 62 nghiên cứu, bao gồm các trích đoạn từ các thử nghiệm lâm sàng được công bố trên tạp chí nổi tiếng quốc tế Lancent, đã được phân tích. Các thử nghiệm lâm sàng này đã sử dụng hơn 500 triệu MSC và trong một số trường hợp lên đến 1 tỷ MSC, xua tan những lầm tưởng và khẳng định năng lực kỹ thuật của HELENE được xếp cùng với các viện nghiên cứu đẳng cấp thế giới.

| Author | Year | Location | Dose | |
|---|---|---|---|---|
| Hess | 2017 | USA | 1200×106 cells | 1tỉ 200 triệu tế bào gốc |
| Bartunek | 2013 | Belgium | 600 -1200×106 cells | 600-1 tỉ 200 triệu tế bào gốc |
| Chanbers | 2017 | Australia | 1×109 cells | 1tỉ 000 triệu tế bào gốc / Rối loạn phổi |
| Steinberg | 2017 | USA | 1×109 cells | 1tỉ 000 triệu tế bào gốc / Đột quỵ |
| Igresias | 2021 | Mexico | 1×109 cells | 1tỉ 000 triệu tế bào gốc / Rối loạn phổi |
| Matsuoka | 2024 | Japan | 1-2×109 cells | 2tỉ 000 triệu tế bào gốc / Chống lão hóa |
Một lượng lớn dữ liệu lâm sàng cho thấy rằng MSC liều thấp thậm chí có thể không hiệu quả trong một số trường hợp, vì chúng tôi không thể tìm thấy trường hợp sử dụng liều thấp tế bào cho các bệnh cụ thể. Trong tương lai gần, cùng với sự cập nhật các dữ liệu khoa học và tài liệu nghiên cứu, chúng tôi sẽ liên tục cải thiện phác đồ điều trị MSC, mục tiêu điều trị, nguồn cung cấp, phác đồ nuôi cấy, sự khác biệt về liều lượng, v.v. để so sánh một cách rõ ràng hơn kết quả của các thử nghiệm lâm sàng có liên quan và các phác đồ này nên được chuẩn hóa. Trước đó, HELENE đã phát triển một chương trình tái trị liệu với lượng tế bào và exosome khác nhau tùy theo độ tuổi, thể trạng và bệnh tật của bệnh nhân, chúng tôi không ngừng cải tiến phương pháp trị liệu để đảm bảo điều trị bằng tế bào gốc tốt nhất với sự an toàn tuyệt đối.
[Trích dẫn] The safety of MSC therapy over the past 15 years: a meta-analysis.
https://doi.org/10.1186/s13287-021-02609-x

| Consultation hours | 10:00~19:00 |
|---|---|
| Closed days | Wednesday · Sunday |
| Address | 〒107-0062 5-9-15 Minami Aoyama, Minato-ku, Tokyo Aoyama OHMOTO Building 3F |
| Tel | 03-3400-2277 |