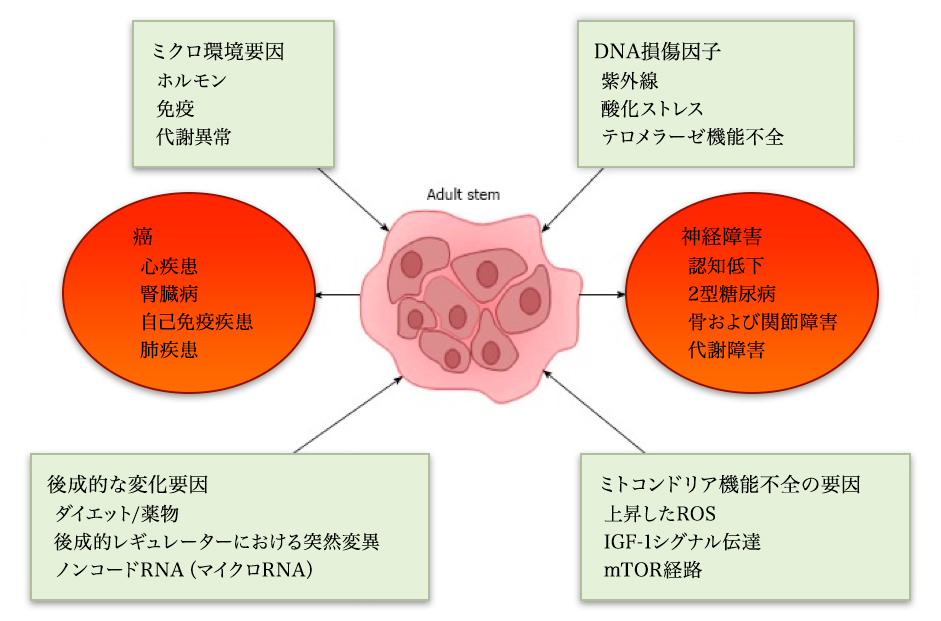
مبدأ MSC (الخلايا الجذعية الوسيطة)
آثار زرع MSC على اعتلال عضلة القلب السكري. (أ) تعمل MSCs على زيادة تنشيط MMP-2 ، وقمع تنشيط MMP-9 ، وتخفيف إعادة تشكيل القلب. (ب) تولد MSCs VEGF و IGF-1 و AM و HGF وتحفز تكوين العضل وتكوين الأوعية في عضلة القلب المصابة. (ج) تعمل MSCs على تحسين نضح عضلة القلب وتجديد عضلة القلب من خلال التمايز إلى خلايا عضلة القلب وخلايا بطانة الأوعية الدموية. الاختصارات: AM ، الأدرينوميدولين ؛ HGF ، عامل نمو خلايا الكبد ؛ IGF-1 ، عامل النمو الشبيه بالأنسولين -1 ؛ MMP ، البروتين المعدني المصفوف ؛ MSC ، الخلايا الجذعية الوسيطة ؛
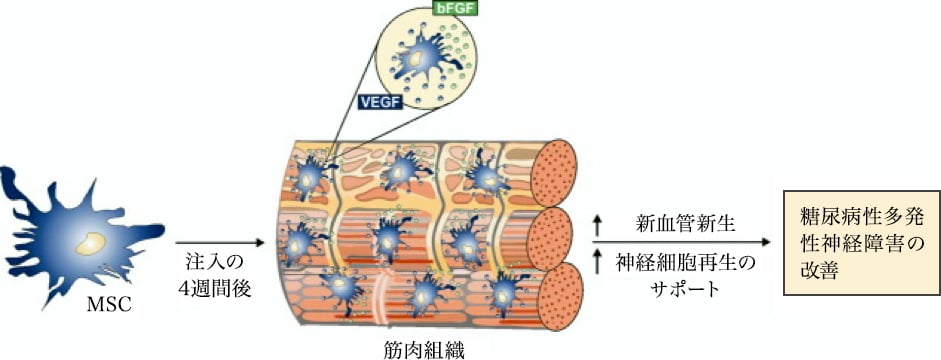
تأثير علاج MSC على اعتلال الأعصاب السكري. بعد أربعة أسابيع من الحقن العضلي ، تترسب الخلايا الجذعية السرطانية في فجوات ألياف العضلات من خلال إنتاج bFGF و VEGF ، مما يؤدي إلى تكوين الأوعية الدموية ودعم تجديد الخلايا العصبية مما يؤدي إلى تحسين اعتلال الأعصاب السكري. الاختصارات: bFGF ، عامل نمو الخلايا الليفية الأساسي ؛ MSC ، الخلايا الجذعية اللحمية المتوسطة ؛ VEGF ، عامل نمو بطانة الأوعية الدموية
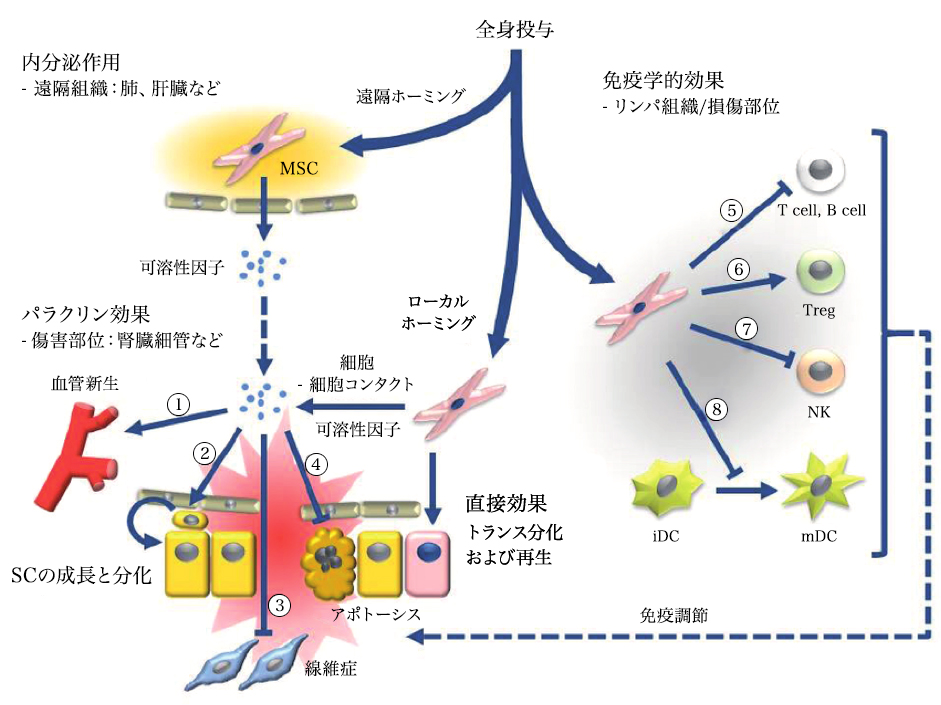
يمكن أن يؤدي إعطاء الخلايا الجذعية الوسيطة بشكل جهازي إلى إحداث تأثيرات غدية صماء أو تأثيرات موضعية نظيرة، بما في ذلك التأثيرات التي تتوسطها الخلايا: 1) عامل نمو بطانة الأوعية الدموية (VEGF)، وعامل النمو الشبيه بالأنسولين 1 (IGF-1)، والبروتين الجاذب للخلايا الوحيدة 1 (MCP1)، وعامل نمو الخلايا الليفية الأساسي (bFGF)، والإنترلوكين 6 (IL-6)؛ 2) تكاثر وتمايز الخلايا الجذعية: عامل الخلايا الجذعية (SCF)، وعامل تثبيط اللوكيميا (LIF)، وعامل تحفيز مستعمرات البلاعم (MCSF)، والعامل المشتق من الخلايا السدوية 1 (SDF1)، والأنجيوبويتين 1، والأكتيفين A؛ 3) تثبيط التليف: عامل نمو الخلايا الكبدية (HGF)، وbFGF، والأدرينوميدولين (ADM)؛ و4) تثبيط موت الخلايا المبرمج: VEGF، HGF، IGF-1، عامل النمو المحول (TGF)-β، bFGF، عامل تحفيز مستعمرات الخلايا المحببة والبلعمية (GM-CSF)، أكتيفين A، وثرومبوسبوندين 1. تشمل التأثيرات المناعية (5-8): 5) تثبيط الخلايا التائية والبائية: مستضد الكريات البيضاء البشرية G5 (HLA G5)، HGF، إنزيم أكسيد النيتريك القابل للتحفيز (iNOS)، إنزيم إندولامين 2،3-ديوكسيجيناز (IDO)، بروستاجلاندين E2 (PGE2)، bFGF، وTGFβ؛ 6) تحفيز تمايز وتكاثر الخلايا التائية التنظيمية (Tregs) من خلال التعبير عن TGFβ؛ 7) تثبيط الخلايا القاتلة الطبيعية (NK) من خلال إفراز IDO، PGE2، وTGFβ؛ ٨) تثبيط نضوج الخلايا المتغصنة (DC) من خلال إفراز البروستاغلاندين E2 (PGE2).
الشكل "Stem Cell Res Ther" مأخوذ من كاريون وفيغيروا. ١١ مايو ٢٠١١؛ ٢(٣): ٢٣.
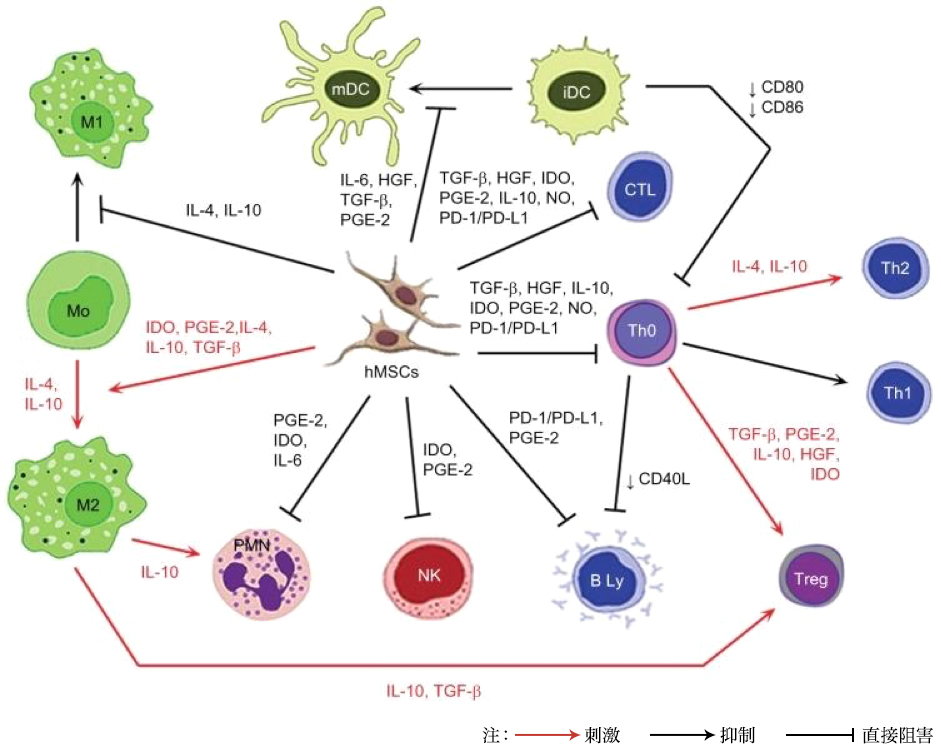
ملاحظة: السهم الأحمر: تحفيز؛ السهم الأسود: تثبيط؛ السهم غير المتصل: تثبيط مباشر.
الاختصارات: iDC، خلية متغصنة غير ناضجة؛ IL، إنترلوكين؛ HGF، عامل نمو الخلايا الكبدية؛ TGF-β، عامل النمو المحول بيتا؛ PGE-2، بروستاجلاندين E2؛ IDO، إندولامين 2،3-ديوكسيجيناز؛ NO، أكسيد النيتريك؛ PD-L1، الرابط 1 للموت المبرمج؛ hMSC، خلية جذعية لحمية متوسطة بشرية؛ Treg، خلية تائية تنظيمية؛ Th، خلية تائية مساعدة؛ CTL، خلية تائية سامة؛ mDC، خلية متغصنة ناضجة؛ PD-1، بروتين 1 للموت الخلوي المبرمج؛ PMN، كريات الدم البيضاء متعددة النوى؛ NK، خلية قاتلة طبيعية
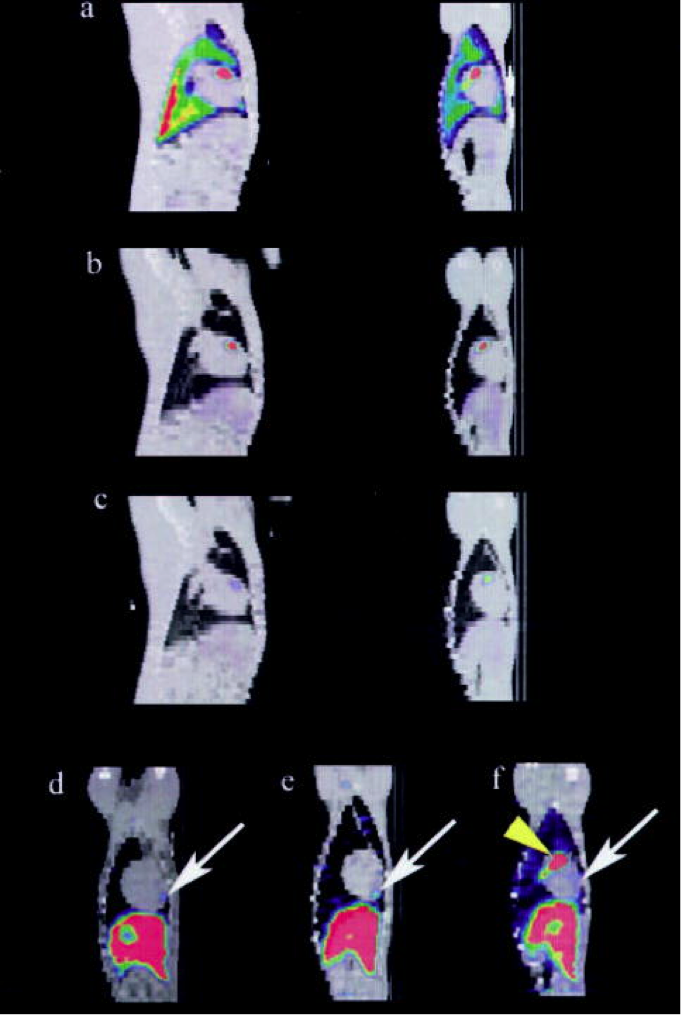
مستوي سهمي (يسار) وصور SPECT / CT مدمجة في الأيام 1 (أ) و 2 (ب) و 7 (ج) تُظهر الامتصاص المحلي في المنطقة البطينية الأمامية لقلب الحيوان الشكل 2 هو منظر للطائرة الإكليلية ( يمين). في آخر نقطة زمنية للتصوير (أيام 5-8) ، تظهر المنطقة القمية الأمامية لامتصاص MSC (الأسهم) في ثلاثة حيوانات تمثيلية في مناظر تشريحية إكليلية. كان التوزيع الرأسي وراء ذلك موجودًا بغض النظر عما إذا كانت نقطة التركيز البؤرية المبكرة قد لوحظت أم لا. (السهم الأصفر في f فقط)
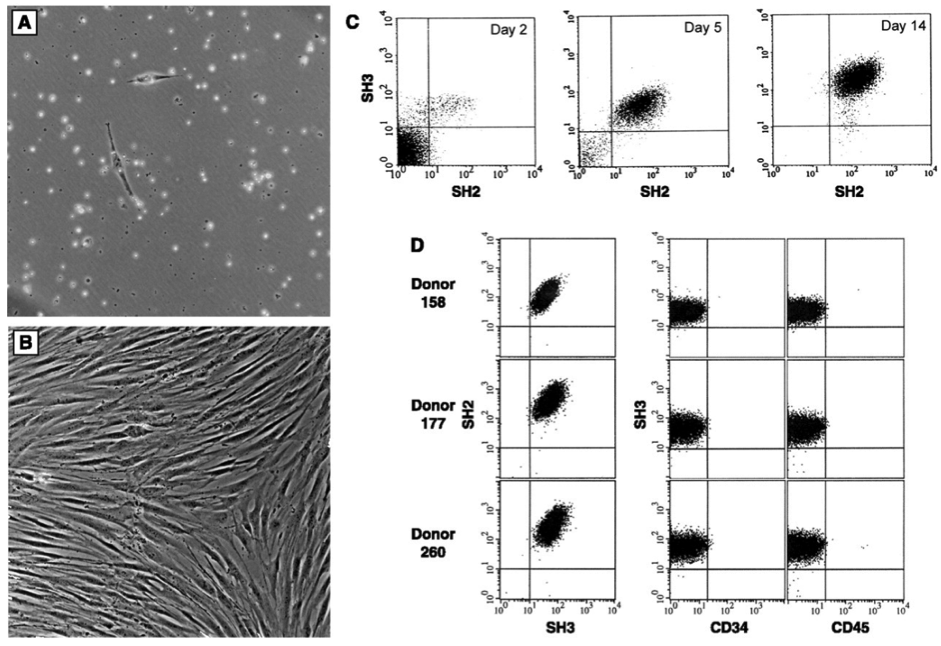
توصيف خلايا انسجة نخاع العظم المعزولة. تم استنبات الخلايا من نخاع العظم بعد تجزئة الكثافة ، كما هو موضح بعد 48 ساعة من الطلاء (أ) و 10 أيام بعد الطلاء (ب). (ج) يظهر قياس التدفق الخلوي إثراء هذه الخلايا في الثقافة. تم الحصول على النتائج في الأيام 2 و 5 و 14 من الثقافة باستخدام الأجسام المضادة SH2 و SH3 المرتفعة مقابل الواسمات السطحية. (11) في اليوم 14 ، كانت الخلايا متجانسة وسلبية بنسبة 95-99٪ للتفاعل مع المستضدات CD14 أو CD34 (Becton-Dickinson) أو CD45 (Pharmingen) الشائعة في خلايا النسب المكونة للدم. (د) تجلى التجانس واستنساخ إجراء العزل عن طريق قياس التدفق الخلوي.