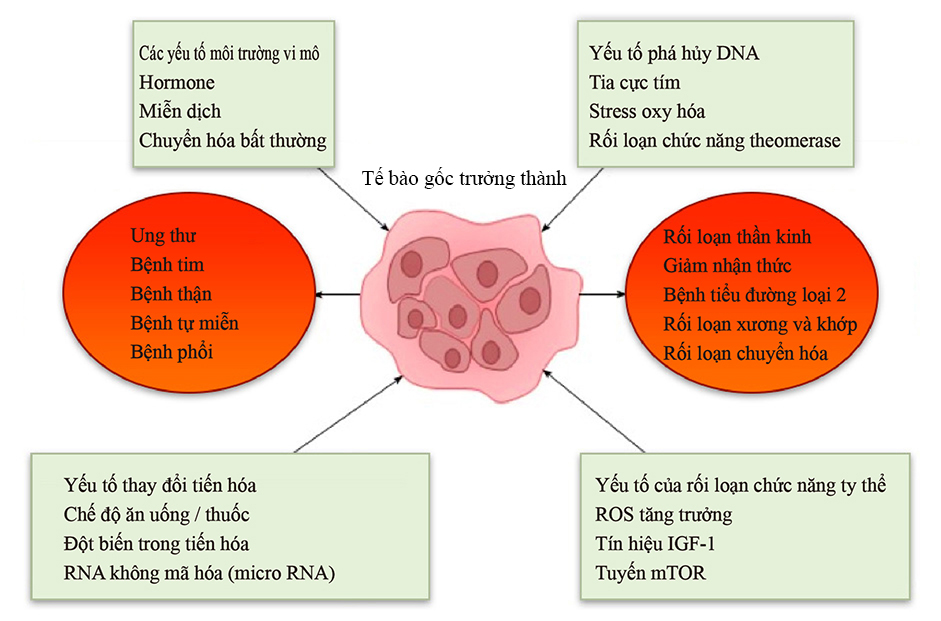
Nguyên lý của MSC
Hiệu quả cấy ghép MSC đối với bệnh cơ tim do tiểu đường. (a) MSC làm tăng cường hoạt động của MMP-2, ức chế hoạt động của MMP-9, giảm thiểu các biến đổi xấu đến tim. (b) MSC sinh ra VEGF, IGF-1, AM, HGF, kích thích sự hình thành mạch máu và hình thành cơ ở cơ tim bị tổn thương. (c) Sau khi phân hóa thành tế bào nội mô mạch máu và tế bào cơ tim, MSC giúp tái sinh cơ tim và cải thiện quá trình lưu thông máu trong cơ tim. Viết tắt: AM (Adrenomedullin), HGF (yếu tố tăng trưởng tế bào gan), IGF-1 (yếu tố tăng trưởng giống Insulin-1), MMP (Matrix metalloprotease), MSC (tế bào gốc trung mô), VEGF (yếu tố tăng trưởng nội mô mạch máu).
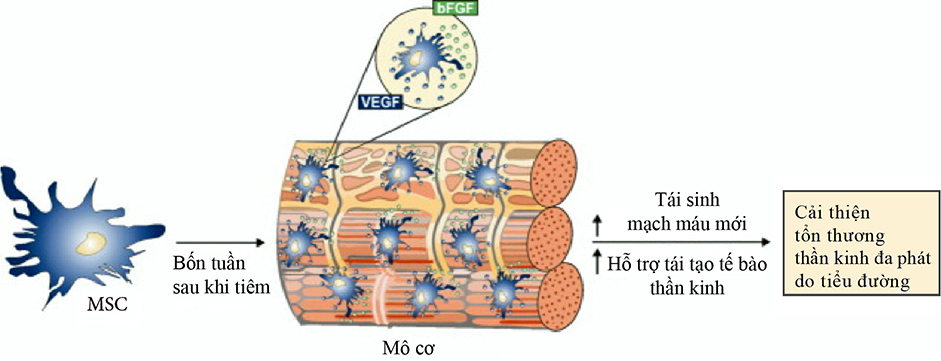
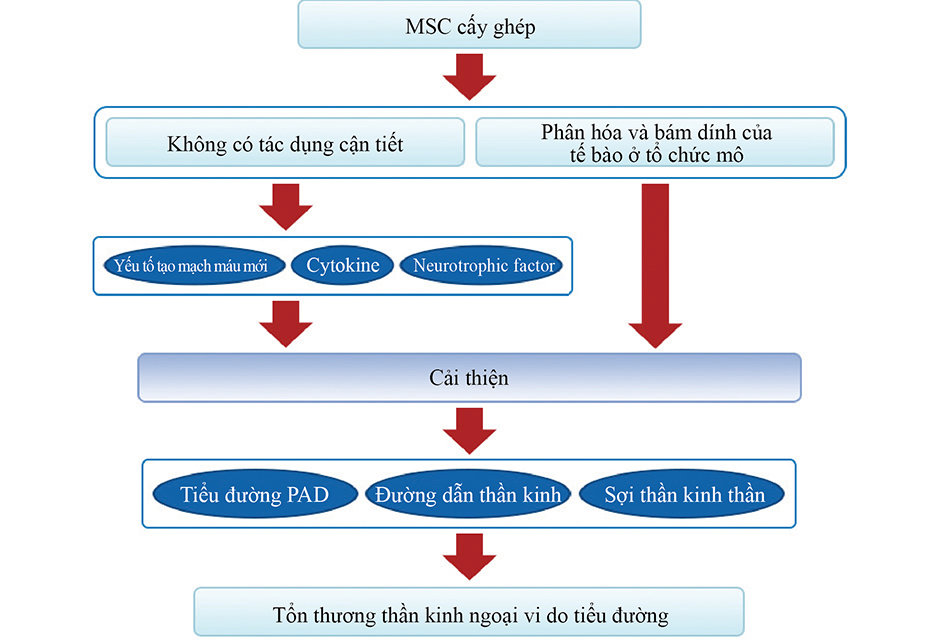
Hiệu quả của liệu pháp MSC đối với bệnh lý thần kinh đa phát do tiểu đường. Sau 4 tuần tiêm vào cơ bắp, MSC sẽ tạo ra VEGF và bFGF, tích lại ở giữa các sợi cơ, hình thành các mạch máu mới, giúp duy trì sự tái sinh của tế bào thần kinh, cải thiện bệnh lý thần kinh đa phát do tiểu đường. Viết tắt: bFGF (yếu tố tăng trưởng nguyên bào sợi cơ bản), MSC (tế bào gốc trung mô), VEGF (yếu tố tăng trưởng nội mô mạch máu).
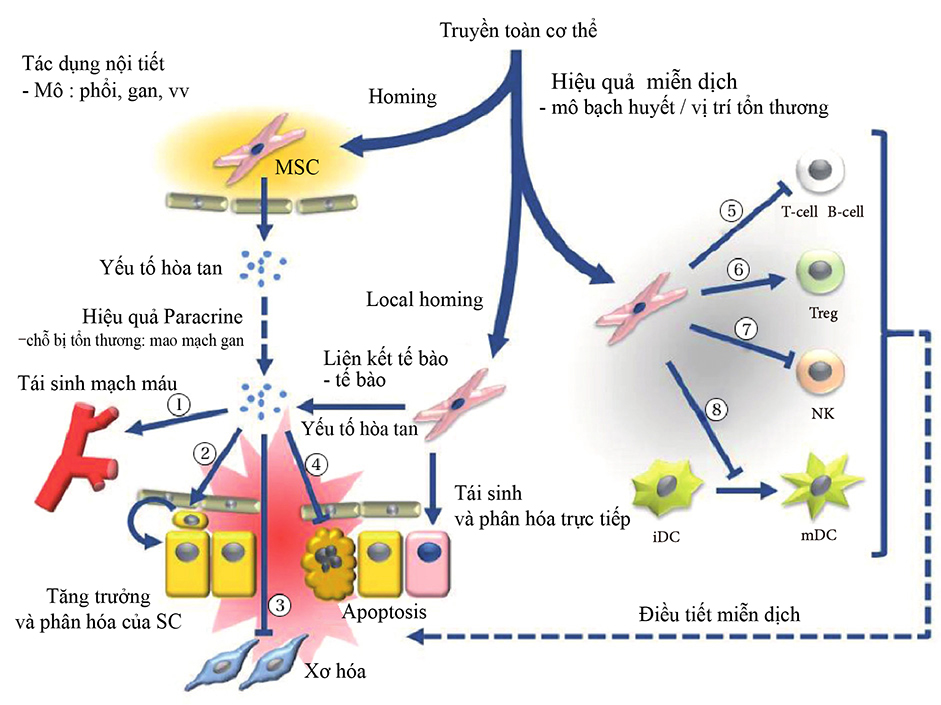
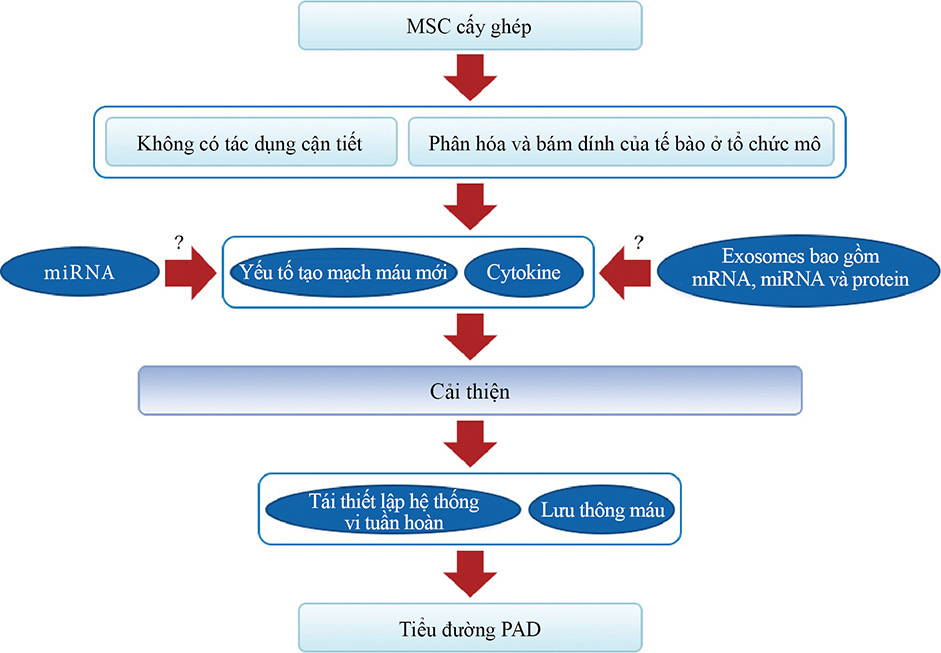
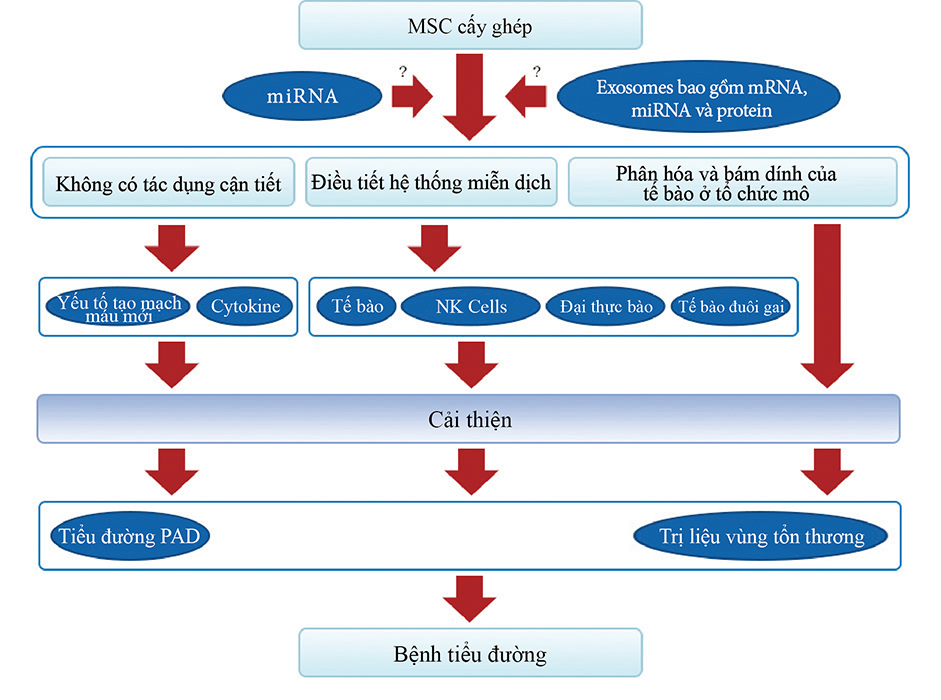
Việc sử dụng tế bào gốc trung mô toàn thân có thể gây ra các tác dụng nội tiết hoặc cận tiết tại chỗ, bao gồm các tác động qua trung gian tế bào: 1) yếu tố tăng trưởng nội mô mạch máu (VEGF), yếu tố tăng trưởng giống insulin 1 (IGF-1), protein thu hút bạch cầu đơn nhân 1 (MCP1), yếu tố tăng trưởng nguyên bào sợi cơ bản (bFGF), interleukin 6 (IL-6); 2) sự tăng sinh và biệt hóa tế bào gốc: yếu tố tế bào gốc (SCF), yếu tố ức chế bệnh bạch cầu (LIF), yếu tố kích thích tạo cụm đại thực bào (MCSF), yếu tố dẫn xuất từ tế bào mô đệm 1 (SDF1), angiopoietin 1 và activin A; 3) ức chế xơ hóa: yếu tố tăng trưởng tế bào gan (HGF), bFGF và adrenomedullin (ADM). và 4) ức chế apoptosis: VEGF, HGF, IGF-1, yếu tố tăng trưởng chuyển đổi (TGF)-β, bFGF, yếu tố kích thích tạo cụm tế bào bạch cầu hạt-đại thực bào (GM-CSF), activin A và thrombospondin 1. Các tác dụng trung gian miễn dịch bao gồm (5-8): 5) Ức chế tế bào T và B: kháng nguyên bạch cầu người G5 (HLA G5), HGF, nitric oxide synthase cảm ứng (iNOS), indoleamine 2,3-dioxygenase (IDO), prostaglandin E2 (PGE2), bFGF và TGFβ; 6) Gây cảm ứng biệt hóa và tăng sinh tế bào T điều hòa (Tregs) thông qua biểu hiện TGFβ; 7) Ức chế tế bào tiêu diệt tự nhiên (NK) thông qua tiết IDO, PGE2 và TGFβ; 8) Ức chế sự trưởng thành của tế bào dendritic (DC) thông qua tiết PGE2.
Hình "Stem Cell Res Ther" được tái bản bởi Carrión và Figueroa. 11 tháng 5 năm 2011;2(3):23.
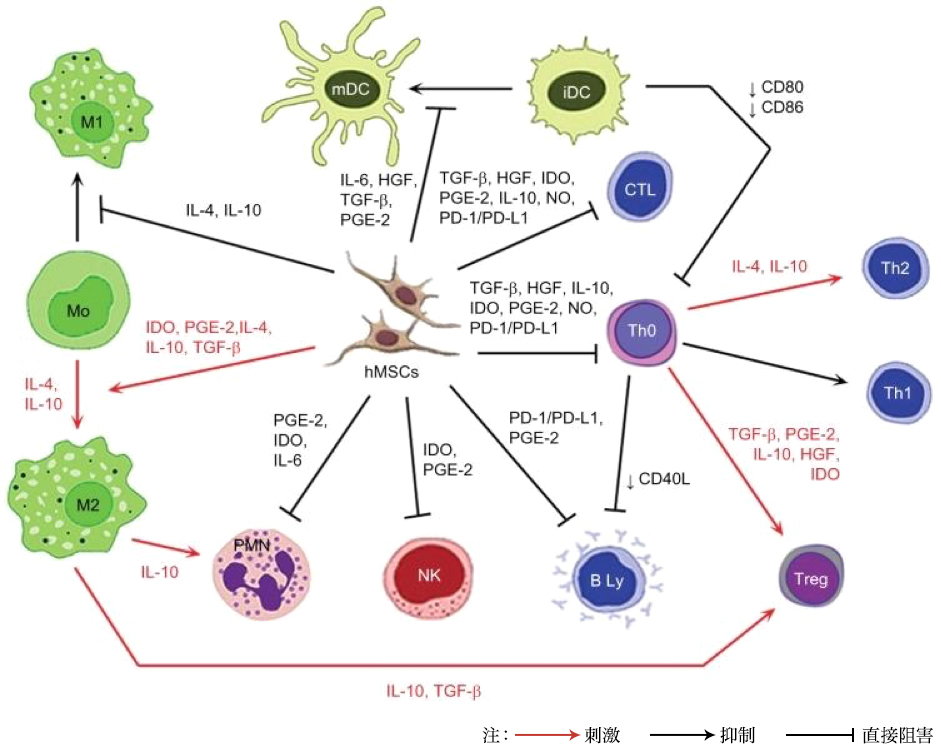
Lưu ý: Mũi tên đỏ: kích thích; mũi tên đen: ức chế; mũi tên không móc: ức chế trực tiếp.
Viết tắt: iDC, tế bào dendritic chưa trưởng thành; IL, interleukin; HGF, yếu tố tăng trưởng tế bào gan; TGF-β, yếu tố tăng trưởng chuyển dạng β; PGE-2, prostaglandin E2; IDO, indoleamine 2,3-dioxygenase; NO, oxit nitric; PD-L1, phối tử chết theo chương trình 1; hMSC, tế bào gốc trung mô người; Treg, tế bào T điều hòa; Th, tế bào T hỗ trợ; CTL, tế bào T gây độc; mDC, tế bào dendritic trưởng thành; PD-1, protein chết tế bào theo chương trình 1; PMN, bạch cầu đa nhân trung tính; NK, tế bào NK
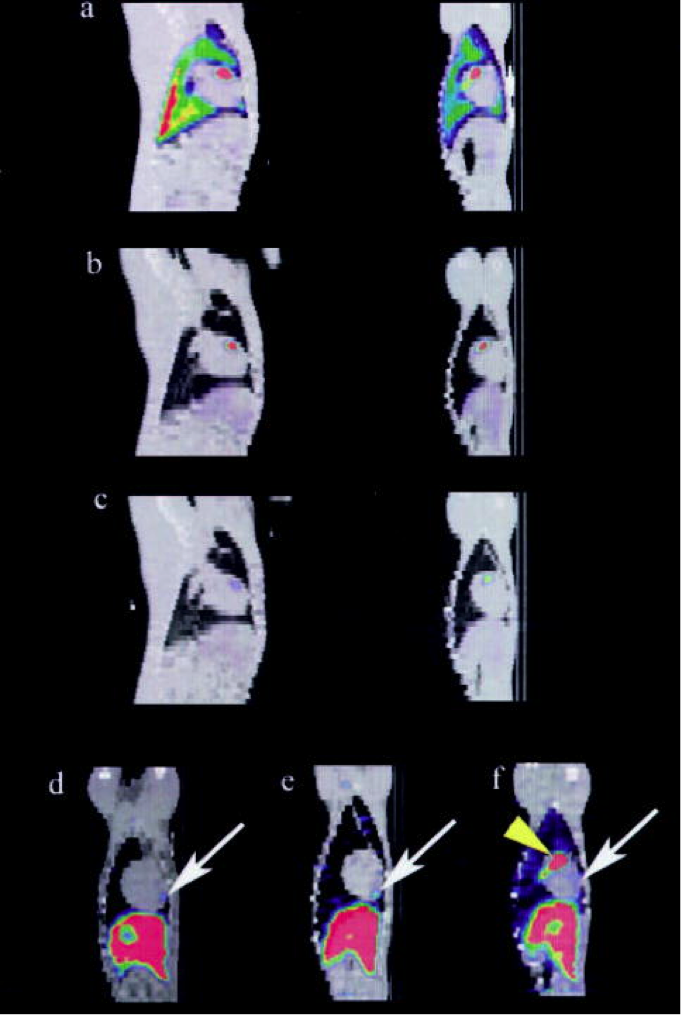
Hình ảnh mặt cắt trước ( bên phải), mặt cắt dọc ( bên trái) của kết quả chụp SPECT/ CT, thể hiện sự hấp thụ ngày 1 ( a), ngày 2 ( b), ngày 7 ( c) tại tâm thất trước của tim động vật. Hình ảnh cuối chụp thời điểm ngày thứ 5 ~ 8, khu vực hấp thụ MSC (mũi tên) thể hiện trên ảnh chụp mặt cắt bên của 3 đại điện.
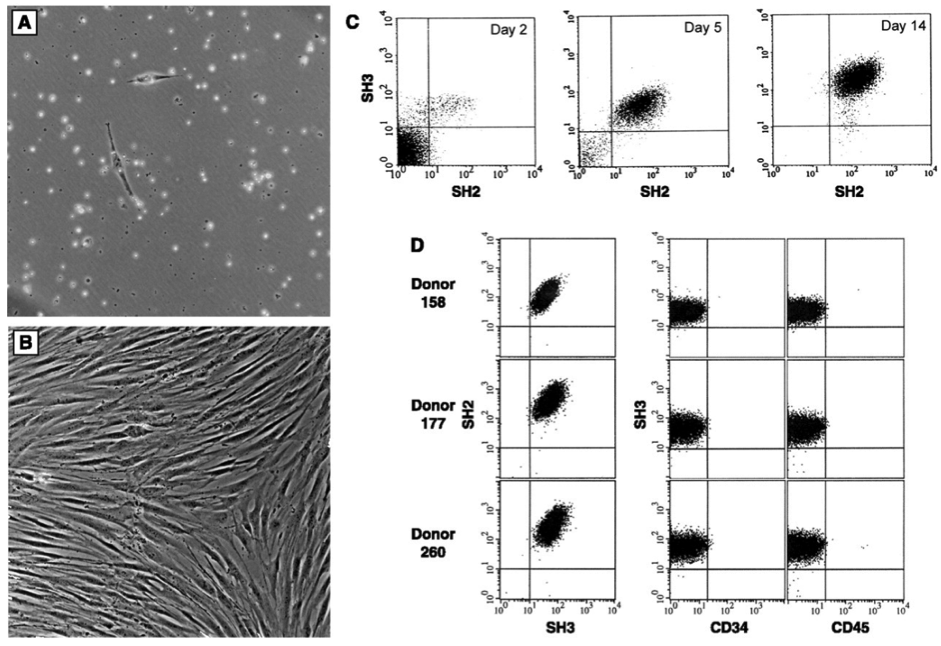
Đặc trưng của tế bào tủy xương đơn tách. Tế bào sau khi phân đoạn mật độ được nuôi cấy từ tủy sống (A) sau 48 tiếng (B) sau 10 ngày (C) Đo dòng tế bào : biểu thị độ tập trung của những tế bào đã được nuôi cấy. Kết quả nuôi cấy ngày thứ 2 , 5 và 14 sau khi sử dụng kháng thể SH3 và SH2 xuất hiện trên các dấu hiệu bề mặt. Vào ngày thứ 14, các tế bào sẽ đồng nhất đến khoảng 95~99%, phản ứng âm tính đối với kháng thể CD45 (Pharmingen), hoặc CD14, CD31 (Becton- Dickinson) thông qua tế bào tạo máu. (D) Khả năng tái hiện và tính đồng nhất trong quá trình phân tách được ly được chứng thực bằng phương pháp đo dòng tế bào.